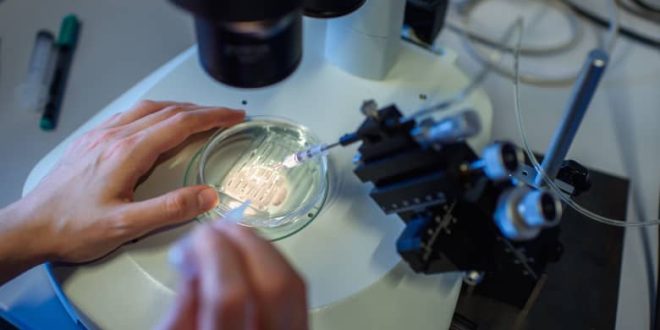
أصبحت المملكة المتحدة أول دولة تمنح الموافقة التنظيمية لعلاج طبي يتضمن أداة تعديل الجينات الثورية “كريسبر”.
وقالت وكالة تنظيم الأدوية ومنتجات الرعاية الصحية في البلاد الخميس، إنها أعطت الضوء الأخضر لعلاج “Casgevy” الذي سيتم استخدامه لعلاج مرض فقر الدم المنجلي والثلاسيميا بيتا. تنجم الحالتان الوراثيتان عن أخطاء في جينات الهيموغلوبين الذي تستخدمه خلايا الدم الحمراء لنقل الأكسجين إلى جميع أنحاء الجسم. وما من علاج معروف عالميًا لأي من الاضطرابين.
يُعد مرض فقر الدم المنجلي، الذي يمكن أن يؤدي إلى نوبات من الألم المنهك، أكثر شيوعًا لدى الأشخاص الذين لديهم جذور عائلية أفريقية أو كاريبية. وقال البيان إن بيتا ثلاسيميا يصيب بشكل رئيسي الأشخاص من منطقة البحر الأبيض المتوسط، وجنوب آسيا، وجنوب شرق آسيا، والشرق الأوسط.
وقال جوليان بيتش، المدير التنفيذي المؤقت لجودة الرعاية الصحية والوصول إليها لدى هيئة تنظيم الأدوية ومنتجات الرعاية الصحية، إنّ “فقر الدم المنجلي والثلاسيميا بيتا مرضان مؤلمان يستمران مدى الحياة ويتسببان بالوفاة في بعض الحالات. إن عملية زرع نخاع العظم التي يجب أن تأتي من متبرع متطابق بشكل وثيق وتنطوي على خطر الرفض، كانت حتى الآن الخيار العلاجي الدائم الوحيد”.
وتابع: “يسعدني أن أعلن أنّنا سمحنا باستخدام علاج مبتكر والأول من نوعه لتعديل الجينات يُسمى Casgevy، الذي تبين خلال التجارب أنه يعيد إنتاج الهيموجلوبين الصحي لدى غالبية المشاركين المصابين بمرض فقر الدم المنجلي وعمليات نقل الدم المعتمدة لمرضى بيتا ثلاسيميا، مخفّفًا من أعراض المرض”.
كريسبر-كاس 9.. الأمل
تتيح تقنية تعديل الجينات”CRISPR-Cas9″ للعلماء إجراء تغييرات دقيقة للغاية على الحمض النووي. فاز المخترعان اللذان قاما بها، أي إيمانويل شاربنتييه وجنيفر أ. دودنا، بجائزة نوبل للكيمياء عام 2020.
وعلاج “Casgevy” ليس حبة أو حقنة بسيطة. يتم العلاج، الذي تصنعه شركة “Vertex Pharmaceuticals”، من خلال أخذ الخلايا الجذعية من نخاع عظم المريض وتعديل جين بالخلايا في المختبر. يجب على المرضى بعد ذلك الخضوع لـ “علاج تكييفي” يمكن أن يشمل دواء مثبط للمناعة، أو علاج إشعاعي أو علاج كيميائي، لتحضير النخاع العظمي قبل إعادة زرع الخلايا المعدلة في المريض، وفقًا لوكالة تنظيم الأدوية ومنتجات الرعاية الصحية.
وجاء في البيان أيضًا، أنه “بعد ذلك، قد يحتاج المرضى إلى قضاء شهر بالحد الأدنى في المستشفى بينما تستقر الخلايا المعالجة في النخاع العظمي وتبدأ بتكوين خلايا الدم الحمراء على النحو المستقر من الهيموجلوبين”.
وتعمل إدارة الغذاء والدواء الأمريكية على تقييم العلاج عينه، ومن المتوقع أن تتخذ قرارًا بشأن سماح استخدامه أو لا بحلول الثامن من ديسمبر/ أيلول.
وأفادت ألينا بانس، المحاضرة الأولى بعلم الوراثة في جامعة هيرتفوردشاير، ببيان أصدره مركز الإعلام العلمي أنها “خطوة عظيمة في تقدم الأساليب الطبية لمعالجة الأمراض الوراثية التي لم نعتقد أبدًا أنه في يمكن علاجها”.
وأضافت بانس أن “تعديل الخلايا الجذعية من النخاع العظمي للمريض يتجنب المشاكل المرتبطة بالتوافق المناعي، أي البحث عن متبرعين متطابقين مع المريض ومتابعة تثبيط المناعة، ويعتبر بمثابة علاج حقيقي للمرض وليس دواء”.
ولم يذكر البيان الصادر عن الوكالة تكلفة العلاج، لكن يرجح أن يكون مكلفًا.
وكان يتمتع “CRISPR-Cas9” بأثر كبير على أبحاث الطب الحيوي، والطب السريري، والزراعة، ويُستخدم على نطاق واسع في المختبرات حول العالم.
وأثارت هذه التكنولوجيا المتطورة جدلًأ بعدما أعلن العالم الصيني هي جيانكوي في عام 2018، أنه أنشأ أول أطفال معدلين وراثيا في العالم. ويقول العلماء إن هذه التقنية القوية لا ينبغي أن تستخدم لمعالجة الجينات البشرية التي ستنتقل من جيل إلى جيل.
 وكالة الموقف العراقي وكالة اخبارية اعلامية دولية
وكالة الموقف العراقي وكالة اخبارية اعلامية دولية